Une étape réglementaire majeure pour Viasonix
Il s’agit là d’une nouvelle étape réglementaire majeure pour l’entreprise, qui démontre son engagement à fournir à ses clients des produits de la plus haute qualité.
Le processus de certification CE du règlement relatif aux dispositifs médicaux (MDR) est beaucoup plus complexe que celui de l’ancienne directive relative aux dispositifs médicaux (MDD). En effet, le RIM impose des exigences plus strictes en matière d’évaluation clinique, de surveillance après la mise sur le marché et de rapports de vigilance, ce qui nécessite davantage de ressources et de données. En outre, le MDR exige la démonstration d’une approche systématique et holistique de la gestion des risques tout au long du cycle de vie du produit.
Le processus de classification du RIM est également plus rigoureux, car il tient compte de la destination, de la conception et des procédés de fabrication d’un dispositif pour déterminer sa classification de risque. En outre, dans le cadre du RIM, les organismes notifiés ont des responsabilités accrues en matière d’audit et de suivi du processus d’évaluation de la conformité. Tous ces facteurs contribuent à rendre la procédure de certification MDR CE beaucoup plus complexe et longue que la procédure MDD CE.
L'impact de la certification MDR sur les marchés européens des dispositifs médicaux
Des entreprises et des produits ont été retirés du marché européen en raison des nouvelles exigences de certification MDR. Le passage au MDR a eu pour conséquence que de nombreuses entreprises ont éprouvé des difficultés à répondre aux exigences plus strictes et à prouver leur conformité aux nouvelles réglementations.
Certaines entreprises ont subi des retards dans l’obtention de la certification MDR, tandis que d’autres n’ont pas été en mesure de répondre aux nouvelles exigences, ce qui a entraîné le retrait de leurs produits du marché européen.
Le MDR impose également aux entreprises de démontrer une approche systématique et holistique de la gestion des risques, ce qui peut s’avérer difficile pour certaines d’entre elles. Le RIM vise à garantir la sécurité et l’efficacité des dispositifs médicaux pour les patients européens. Néanmoins, la transition a été difficile pour certaines entreprises. Cela a entraîné la perte temporaire de certains produits sur le marché.
Néanmoins, Viasonix est fière de faire partie de l’élite des entreprises qui ont achevé avec succès le processus MDR sans avoir besoin d’une extension et qui peuvent continuer à introduire leurs produits sur les marchés européens pour de nombreuses années à venir.
Produits Viasonix approuvés MDR
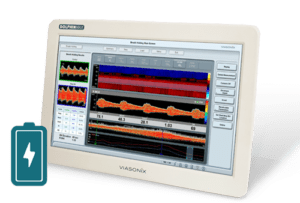
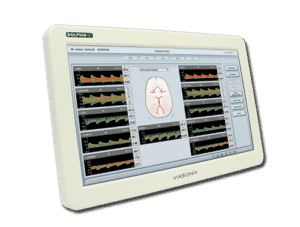
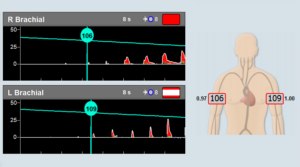
Le système physiologique vasculaire Falcon et l’appareil de doppler transcrânien Dolphin sont deux des produits phares de Viasonix. Ces deux appareils sont désormais approuvés par le MDR. Ils sont conçus pour fournir des informations diagnostiques aux professionnels de la santé, afin de les aider à prendre des décisions éclairées concernant le traitement et les soins de leurs patients.
Le système physiologique Falcon est utilisé pour le diagnostic vasculaire de routine et le diagnostic clé, tandis que la machine Dolphin est utilisée pour le diagnostic non invasif et la surveillance du flux sanguin cérébral.
Sélection de produits approuvés dans le cadre du MDR
Assurer la continuité de l'approvisionnement en produits
Viasonix a travaillé sans relâche pour s’assurer que ses produits répondent aux exigences rigoureuses du MDR européen. Ce processus de certification est conçu pour évaluer la sécurité, la performance et la qualité des dispositifs médicaux, garantissant ainsi que seuls les meilleurs produits arrivent sur le marché.
L’obtention du certificat européen MDR témoigne du dévouement et du travail acharné de l’équipe d’ingénieurs, de techniciens et de spécialistes du contrôle de la qualité de Viasonix. Leur expertise et leur souci du détail ont permis de créer des produits non seulement très efficaces, mais aussi sûrs et fiables.
En outre, nos nombreux distributeurs et partenaires commerciaux européens peuvent continuer à vendre nos produits vasculaires et TCD dans leurs pays respectifs.
Conclusion
Viasonix continuera à innover et à développer des technologies médicales nouvelles et améliorées. L’objectif de l’entreprise sera toujours de fournir les meilleurs soins possibles aux patients et de veiller à ce que les professionnels de la santé disposent des outils dont ils ont besoin pour diagnostiquer et traiter efficacement leurs patients.
En conclusion, la réussite du processus de certification MDR européen constitue une avancée majeure pour Viasonix. Il témoigne de l’engagement de l’entreprise à fournir des produits de la plus haute qualité à ses clients et de sa volonté d’améliorer les soins aux patients.
Pour plus d’informations, veuillez nous laisser un message.